
O INSTITUTO NACIONAL DE CIÊNCIA E TECNOLOGIA EM VACINAS (INCTV) é estruturado em três grandes divisões e um núcleo central. A Divisão de Doenças infecciosas e Imunologia incluindo três áreas principais: (a) imunologia, (b) patogênese e imunologia clínica, e (c) interação patógeno-hospedeiro que irão fornecer fundamentação científica para o desenvolvimento de vacinas eficazes. A Divisão de Tecnologia em Vacinas será estruturada em quatro plataformas tecnológicas: (a) descoberta de antígenos, (b) descoberta de adjuvantes, (c) construção de vacinas que incluem sistemas de entrega, e (d) testes de imunogenicidade e provas de conceito. Finalmente, na Divisão de Desenvolvimento de Vacinas, formulações em estágio avançado de desenvolvimento já aprovadas em estudos de prova de conceito pelos laboratórios de pesquisa serão submetidas a testes de segurança em modelos pré-clínicos bem controlados e em ensaios clínicos de fase I. As diferentes divisões do INCT gerarão uma grande quantidade informações que alimentam o Núcleo de Vacinologia de Sistemas. Ao combinar a análise de sistemas com modelos matemáticos e computacionais, esperamos aprimorar nossa compreensão para o desenho racional de novas vacinas e melhoramento das já existentes.
Imunologia – Áreas relevantes para imunidade inata e mediada por células T e B serão abordadas. O foco principal dos nossos pesquisadores é: (i) O papel de receptores da imunidade inata (IIRs) na indução das respostas imunes inata e adaptativa que sejam protetoras durante a infecção microbiana e na vacinação; (ii) o mecanismo pelo qual células T CD8+ matam protozoários parasitos intracelulares e como células citotóxicas de memória específicas contra o patógeno são mantidas em camundongos infectados/vacinados; e (iii) identificação de biomarcadores associados com o desenvolvimento de imunidade protetora mediada por anticorpos.
Patogênese e Imunologia Clínica – Informações sobre o genoma do hospedeiro, associadas a avanços na bioquímica de proteínas e manipulação genética nos permitirão caracterizar mecanismos de resistência à infecção. Para isto, nós estamos caracterizando mudanças globais no padrão de expressão gênica em células ou tecidos de pacientes com as formas clínicas assintomáticas, sintomáticas e graves de COVID19, dengue e malária. Baseado na análise dos dados gerados e aqueles disponíveis em bancos de dados geramos hipóteses, que serão testadas experimentalmente em modelos experimentais e ensaios in vitro com amostras dos pacientes estudados. Estes estudos permitirão a identificação e caracterização de mecanismos imunológicos e celulares de resistência e patogênese da infecção e podem ajudar no desenvolvimento de novas vacinas.
Interação patógeno-hospedeiro – Nós trabalhamos também para definir mecanismos essenciais para a interação entre patógeno e hospedeiro com o objetivo de identificar moléculas derivadas do patógeno que são fatores de virulência. Estes estudos são essenciais para a identificação de antígenos que podem ser utilizados em novas vacinas.
Atualmente, o CNVacinas possui diferentes plataformas tecnológicas para desenvolvimento de testes de diagnósticos e vacinas que permitem reduzir a dependência de fornecedores, conferindo maior agilidade flexibilidade no processo de desenvolvimento desses produtos.
Permite o cultivo bacteriano em frascos e biorreatores para indução de expressão proteínas recombinantes após a inserção, no genoma da bactéria, da sequência de DNA que codifica essa proteína. A otimização do processo é feita por meio do uso de diferentes cepas de E. coli e condições de cultivo, condições de lise celular sob alta pressão e a baixas temperaturas e separação de proteína por centrifugação ou filtração tangencial. Após a etapa de expressão (upstream) é realizado o processo de purificação (dowstream) utilizando diferentes combinações de etapas de cromatografia de afinidade, troca iônica, exclusão molecular etc., seguindo-se o controle de qualidade em conformidade com as normas BPL.
Permite a produção proteínas recombinantes, como, por exemplo, antígenos virais (Dengue, SARS-CoV-2 e Chikungunya) a partir do cultivo de células eucarióticas transformadas geneticamente de forma transiente ou estável. Com essa plataforma, é possível gerar antígenos contendo modificações na proteína que aumentam a sensibilidade em testes de diagnóstico ou eficácia como vacina. Segue-se a isso as etapas de purificação de proteinas e controle de qualidade. A otimização do processo envolve a avaliação da produção das proteínas em células aderentes e em suspensão, métodos de cultivo, condições de expressão, secreção no sobrenadante da cultura e avaliação dos métodos de purificação, em conformidade com as normas BPL.
Permite a construção e produção, em escala piloto, em conformidade com as normas BPL, .de vetores virais recombinantes contendo sequências de antígenos vacinais, como, por exemplo, vacinas contra dengue ou SARS-CoV-2 utilizando vírus MVA ou adenovírus, ou vírus atenuados tais como os utilizados em vacina para monkeypox. Nessa plataforma, além da produção e caracterização dos vetores virais, são realizadas análises para verificação da montagem do vetor, amplificação viral, purificação, testes de estabilidade, quantificação viral e ensaios de imunogenicidade.
Permite a construção de plasmídeos utilizados para o desenvolvimento de vacinas de DNA e para a produção de proteínas recombinantes para produção de vacinas e/ou desenvolvimento de testes diagnóstico em sistemas procarióticos ou eucarióticos. Inclui também a produção e purificação de RNA contendo sequências de antígenos vacinais para várias doenças como COVID-19, doença de Chagas, Dengue e Leishmaniose, e sua formulação, utilizando nanopartículas lipídicas (LNP) para testes de imunogenicidade e proteção necessária ao desenvolvimento de vacinas de RNA.
A plataforma de edição gênica visa gerar patógenos modificados geneticamente utilizando a estratégia de CRISPR/Cas9 com o objetivo de entender a biologia desses patógenos, seus mecanismos de virulência e escape da resposta imune do hospedeiro e, também, com o objetivo de gerar patógenos atenuados que possam ser testados para desenvolvimento de vacinas.
Responsável pela caracterização, identificação e quantificação de proteínas candidatas a novos alvos vacinais, formulações e adjuvantes mediante diversas técnicas como espectrometria de massas de alto desempenho (LC-MS/MS), HPLC e dicroísmo circular. Dotada de uma infraestrutura completa para análises proteômicas (Orbitrap Exploris 240 Thermo, Maldi TOF 8020 Shimadzu), nessa plataforma são realizados a identificação e quantificação de proteínas em misturas complexas, detecção de massa intacta, mapeamento peptídico e sequenciamento da estrutura primária e secundária, identificação de modificações pós-traducionais (PTMs), identificação e quantificação de impurezas relacionadas ao processo de produção, assim como a detecção de alterações conformacionais em proteínas por dicroísmo circular e o monitoramento da desnaturação e enovelamento de proteínas em diferentes condições por medidas de fluorescência.
Permite o desenvolvimento, padronização e realização dos exames que empregam a reação em cadeia da polimerase (PCR) convencional ou quantitativo (Real Time PCR). Permite, ainda, o desenvolvimento de novas metodologias para diagnóstico molecular utilizando os sistemas CRISPR/Cas12 e CRISPR/Cas13, bem como o sequenciamento de DNA pelo método de Sanger e por sequenciamento de nova geração.
Permite a produção e prototipagem de testes imunodiagnósticos (kit de testes ELISA e testes rápidos) para detecção de marcadores decorrentes de infecções de interesse humano e veterinário (antígenos ou anticorpos). Nessa plataforma é feita avaliação da resposta imune humoral e celular em modelos animais e amostras humanas e do potencial de insumos para serem aplicados em testes diagnósticos e vacinas, bem como a determinação da atividade biológica, potência e estabilidade dos antígenos vacinais.
Atua na imunização de animais experimentais utilizando-se de diferentes plataformas vacinais como proteínas recombinantes, DNA, mRNA, adenovírus e influenza recombinantes contra doenças como COVID-19, Doença de Chagas, Malária, Leishmaniose e Dengue. As imunizações podem ser realizadas por via intramuscular, intradérmica, subcutânea ou intranasal. Também atua na avaliação da resposta humoral e celular induzida pela imunização e proteção da formulação vacinal. Os objetivos principais são os ensaios experimentais para testes de imunogenicidade, proteção, assim como testes de toxicidade e segurança, utilizando formulações vacinais produzidas em condições BPL ou BPF.
Permite a realização de ensaios clínicos de candidatos vacinais por meio do planejamento, coordenação e execução dos testes. Com essa plataforma, são feitos os desenhos dos ensaios clínicos, a elaboração de protocolos e documentos acessórios para submissão às agências regulatórias, de testes em humanos, incluindo estudos de fase I (first- -in-human) a fase III. Proporciona a seleção de CRO (Contract Research Organization), centros clínicos, estratégia de recrutamento, o acompanhamento do andamento de ensaios supervisionando, a execução do cronograma e a aderência às resoluções brasileiras de ética em pesquisa e boas práticas clínicas (BPC), bem como a análise de resultados de segurança, imunogenicidade e eficácia.
A equipe dessa plataforma é responsável pelo acompanhamento de todos os projetos, fiscalização de prazos e da documentação, garantindo a eficiência dos processos para obtenção de resultados com elevado grau de excelência. A equipe é encarregada pelo monitoramento da data de validade de insumos e certificação de equipamentos e, de forma geral da manutenção do reconhecimento BPL, obtido junto ao Inmetro, que estabelece documentos normativos que especificam os requisitos para a implementação e manutenção de um Sistema da Qualidade. Essa Garantia da Qualidade segue padrões internacionalmente reconhecidos.
Permite o planejamento e acompanhamento dos processos ligados aos projetos de pesquisa e desenvolvimento de novos produtos de acordo com as normas regulatórias nacionais e internacionais vigentes. A equipe elabora e revisa a documentação como o dossiê de desenvolvimento clínico de medicamento (DDCM); o dossiê específico de ensaio clínico (DEEC), a brochura do investigador (BI) e o plano de estudos. Gerencia as etapas do processo para a submissão da documentação junto à ANVISA e responde às exigências e ofícios recebidos. Presta suporte técnico à equipe de desenvolvimento farmacotécnico e produção dos insumos, por meio de contato com os órgãos regulatórios e avaliação de requisitos específicos não claramente definidos pelas agências buscando agilidade no processo de inovação e submissão a agências regulatórias.

O principal foco do INCT-V são as doenças negligenciadas (leishmaniose, doença de Chagas, e malária causada pelo Plasmodium vivax, assim como as arboviroses Dengue e Zika). Em 2020, os nossos pesquisadores orientaram grande parte de seus esforços para pesquisa sobre a patogênese, diagnóstico e vacina para COVID-19. Além disto, alguns pesquisadores do INCT-V trabalham com Hepatite e Câncer. Entre as vacinas em desenvolvimento mais avançadas estão as vacinas contra leishmaniose visceral humana (A2), malária causada pelo P. vivax (diferentes isoformas da proteína CS), doença de Chagas (ASP2-transialidase) e COVID-19 (proteínas S/N). Todas utilizam proteínas quimeras recombinantes associadas a adjuvantes assim como o vetor viral não-replicante denominado Adenovirus 5 expressando os mesmos antígenos. A vacina contra leishmaniose visceral humana tem como base a Leish-Tec®, uma vacina contra leishmaniose visceral canina que foi desenvolvida por pesquisadores do INCT-V. No caso da vacina para COVID19 temos também formulações vacinais utilizando os virus não-replicativos influenza e MVA expressando as proteínas S e N do SARS-CoV2.
Os kits-diagnósticos (ELISA e teste imunocromatográfico rápido) para leishmaniose humana e canina permitem excluir os resultados de reação cruzada com doença de Chagas, e outras doenças parasitárias. Os mesmos testes estão disponíveis para malária e de doença de Chagas possuindo foco a triagem sorológica em bancos de sangue e estudos de campo, tendo sido desenvolvidos a partir da utilização de antígenos recombinantes. Kits multiteste (em desenvolvimento) de dengue, zika e chikungunya permitirão detectar e diferenciar o material infectado por um dos três vírus.
Finalmente, recebendo um aporte de investimento para o desenvolvimento de tecnologias para atuar no combate ao coronavírus, o CT Vacinas está desenvolvendo uma abordagem completa para atuar na pandemia. Os testes moleculares (RT-PCR) e ELISA já estão prontos. Além disso, pretende-se concluir o desenvolvimento de um teste rápido em até 1 ano e ter uma vacina que previne simultaneamente contra COVID-19 e influenza em até dois anos. Uma vacina que oferece imunização simultânea a esses dois grupos de doenças poderia reduzir significativamente os custos do setor público de saúde.
Durante os últimos nove anos de apoio do Instituto do Milênio (2005-2008) e do INCT (2009-2020), nós submetemos muitos pedidos de patentes relacionadas a processos e produtos de vacinas e testes de diagnóstico, em órgãos nacionais e internacionais nos EUA, União Européia, e outros países da América Latina e Ásia. As patentes estão relacionadas a vacinas contra o câncer, doença de Chagas, dengue, leishmaniose, malária, e toxoplasmose, bem como a plataforma vacinal utilizando o vírus da Febre Amarela (YF17D). Já a maioria das patentes para diagnósticos protegem novos testes de diagnósticos para uso laboratorial e de campo para detectar doença de Chagas, dengue, leishmaniose e toxoplasmose.

Geração da tecnologia Kit ELISA e Teste rápido para COVID-19 em 5 meses no período de pandemia
Transferência da tecnologia para COVID-19 para Bio-Manguinhos
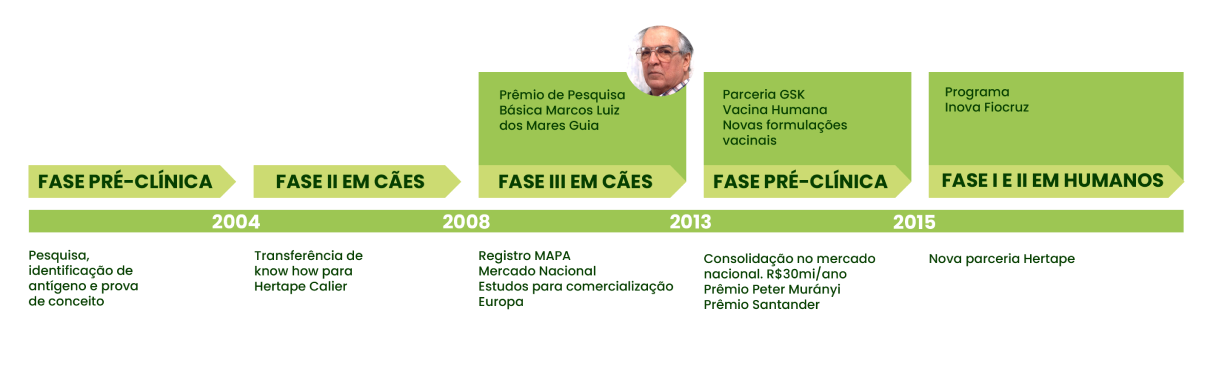
Geração da tecnologia vacina recombinante para leishmaniose visceral canina (Leishtec) – Um modelo nacional de interação Universidade e Indústria privada.
Transferência da tecnologia – Maior royalties cedidos a UFMG e valor econômico na sociedade.
Um dos fortes componentes do INCTV é a formação de pessoal. Durantes os anos de existências já foram formados centenas de pós-doutores, doutores, mestres, e alunos de iniciação científica. Muitos destes alunos estão espalhados em instituições de ensino e pesquisa do Brasil e exterior, muito dos quais se tornaram líderes em suas áreas de ação. Os nossos pesquisadores são orientadores dos cursos de pós-graduação listados abaixo que são licenciados pela CAPES.
Tabela de formação de recursos humanos

O Instituto Nacional de Ciência e Tecnologia de Vacinas (INCTV) tem como missão atuar no desenvolvimento de vacinas contra doenças infecciosas, dando prioridade àquelas que afetam o Brasil e tem sido negligenciadas pela indústria farmacêutica; e contribuir para elevar a pesquisa científica e a tecnologia nas áreas de imunologia e vacinas em nosso país a um patamar de excelência internacional.



















