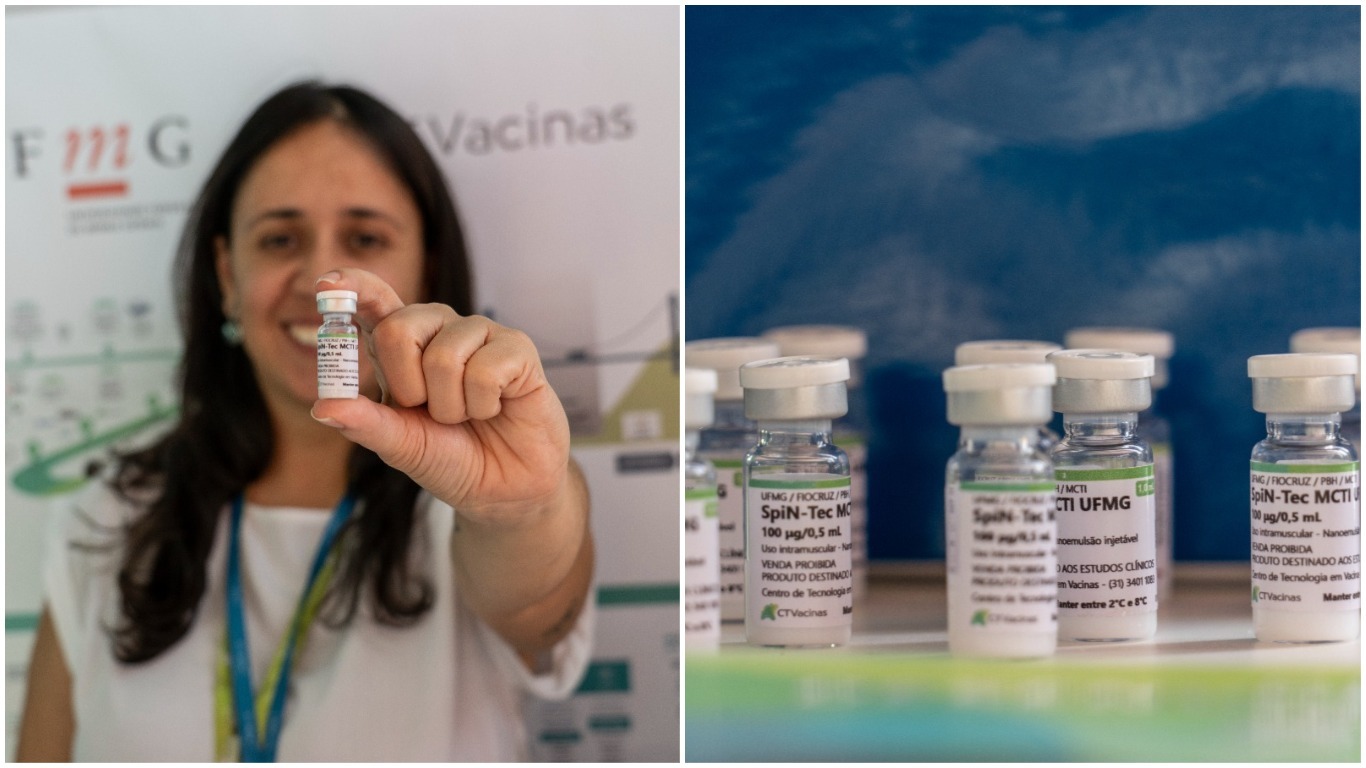
Anvisa libera início da penúltima fase dos testes da SpiN-TEC e UFMG procura voluntários
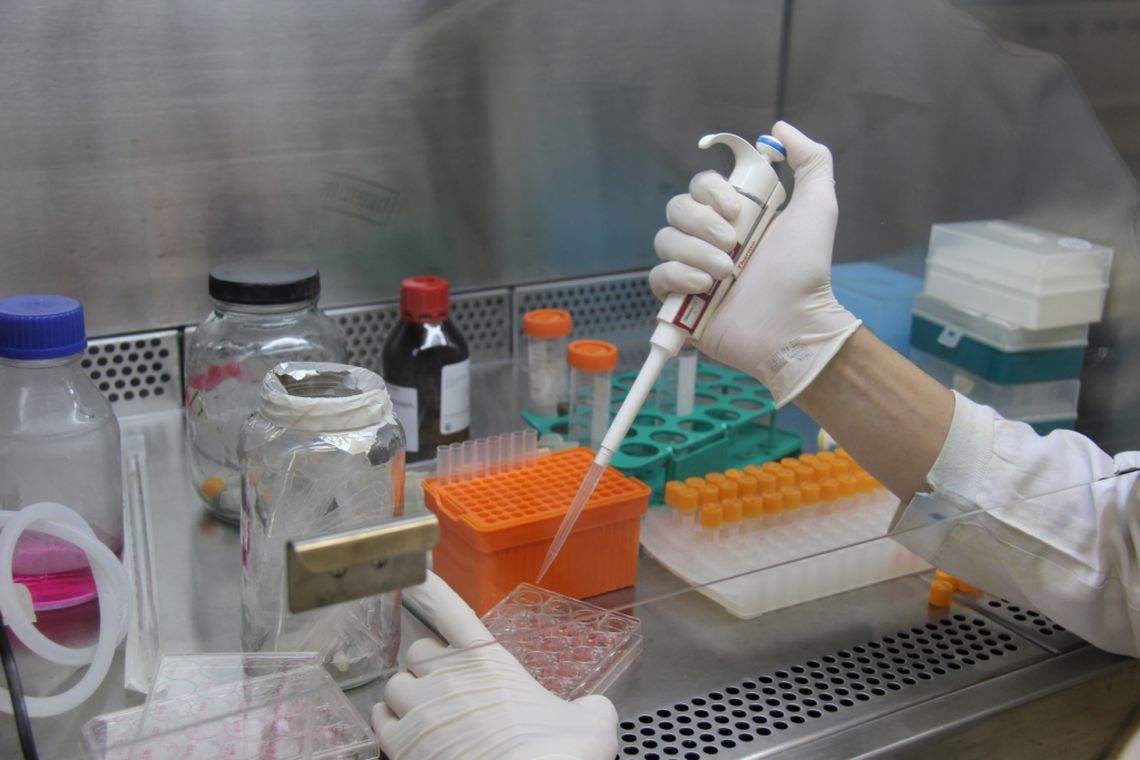
A liberação da Anvisa para o início da fase 2 dos testes clínicos da SpiN-TEC – a primeira vacina 100% brasileira – foi publicada oficialmente nesta quarta-feira (30) no Diário Oficial da União. Com isso, a UFMG e o CTVacinas abrem, instantaneamente, o cadastro de voluntários para mais essa etapa.
>> FAÇA O CADASTRO E CONTRIBUA COM A CIÊNCIA BRASILEIRA
Para participar do recrutamento de voluntários e contribuir com esse importante marco para a ciência brasileira, você deve, apenas, atender aos seguintes critérios:
- possuir entre 18 e 85 anos
- ter recebido as doses iniciais de CoronaVac ou AstraZeneca; e o reforço com Pfizer ou AstraZeneca antes de março (ou seja, há pelo menos 6 meses)
- não ter contraído Covid-19 ou contraído a doença no máximo até março (ou seja, há pelo menos 6 meses)
- ter disponibilidade para participar de acompanhamentos presenciais em Belo Horizonte
Pessoas com doenças crônica controlada (como hipertensão, diabetes e outras) podem se inscrever – elas passarão por uma avaliação médica para conferir se podem ou não participar dos testes clínicos.
Caso você atenda a todos os critérios, faça a sua inscrição AQUI. Se preferir, pode ligar ou chamar no WhatsApp pelo número (31) 99972-0292 – ou, ainda, ligar no telefone (31) 3401-1152.
Mais um marco
A liberação da Anvisa (Agência Nacional de Vigilância Sanitária) oficializa o sucesso da fase 1 dos testes clínicos da SpiN-TEC, cujos resultados preliminares reforçaram que trata-se de uma vacina segura e imunogênica, ou seja, protege o organismo contra a Covid-19.
“É mais um marco para o desenvolvimento desta vacina, um marco para a ciência brasileira, para a UFMG e para o CTVacinas (Centro de Tecnologia de Vacinas). Estamos muito felizes que a SpiN-TEC recebeu aprovação para seguir”, afirma o coordenador dos testes clínicos da vacina, Helton Santiago.

“A gente conta agora, novamente, com a colaboração da população de Belo Horizonte e região para que a pesquisa e o desenvolvimento da vacina continue”, complementa Santiago, que também é diretor clínico do CTVacinas e professor da UFMG.
Como serão os testes?
Dentre as pessoas cadastradas, o CTVacinas e a Unidade de Pesquisa Clínica em Vacinas (UPqVac) da UFMG farão uma triagem para selecionar os voluntários: são 360 para a fase 2.
“Os selecionados, então, serão avaliados clinicamente e laboratorialmente num processo chamado de triagem. Se a pessoa for elegível para o estudo, será convidada a receber a vacina SpiN-TEC. A pessoa vai no dia da vacinação, faz os procedimentos adequados e fica de observação por até 1h. Depois, já está liberada para ir pra casa e faremos o monitoramento ao longo de 1 ano”, explica Helton Santiago.
A equipe que executa os testes clínicos fará ligações periódicas para os voluntários para saber como estão se sentindo. Além disso, as pessoas farão sete visitas programadas ao centro de pesquisa (UPqVac), da Faculdade de Medicina da UFMG, onde a dose será aplicada:
- com 1 semana após a aplicação
- 2 semanas
- 28 dias
- 90 dias (3 meses)
- 180 dias (6 meses)
- 270 dias (9 meses)
- 360 dias (cerca de 1 ano)
Importância dos voluntários
A primeira vacina contra Covid-19 totalmente desenvolvida no Brasil só pode chegar aos braços dos brasileiros após os testes clínicos. Portanto, os voluntários e voluntárias são essenciais para o marco na nossa ciência.
“A SpiN-TEC está conseguindo fechar uma lacuna no desenvolvimento tecnológico no Brasil. Temos ótimos pesquisadores básicos que desenvolvem vacinas, testam em animais e fazem descobertas sensacionais. Também temos ótimos pesquisadores clínicos, que fazem ensaios, testam medicamentos e seguem protocolos gerando dados de grande relevância. Falta essa ponte entre um e outro”, celebra o coordenador dos testes clínicos.
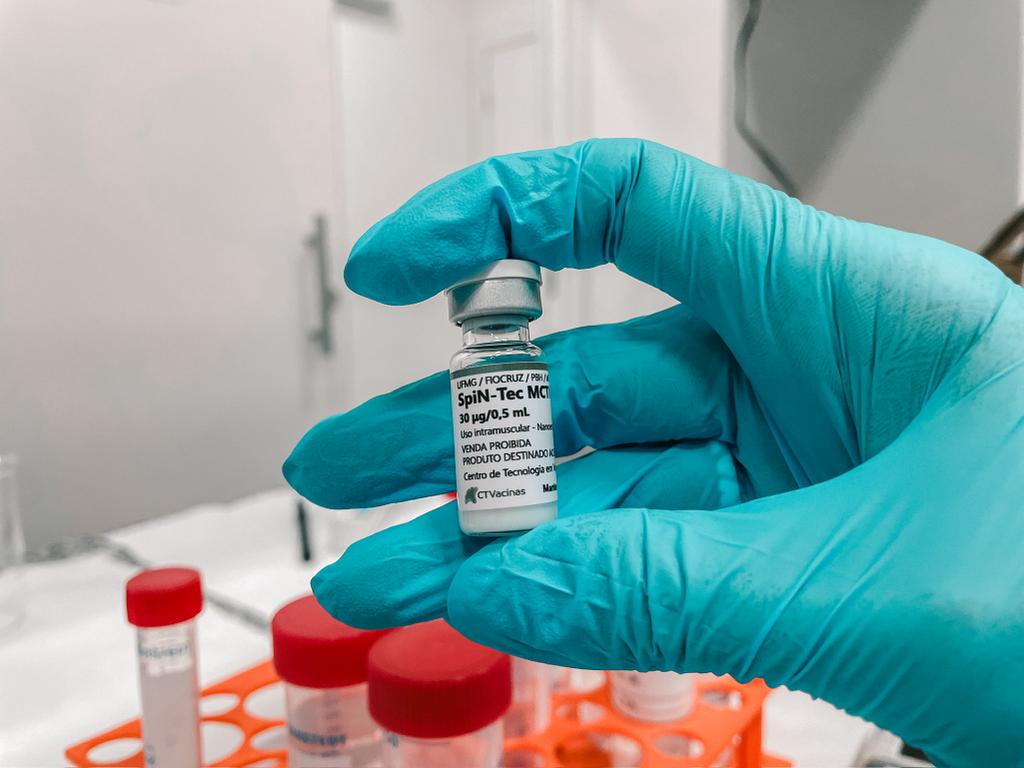
“Faltava superar o chamado vale da morte das inovações. Então, a SpiN-TEC tem possibilitado ao Brasil criar essa expertise: transferir conhecimento da equipe básica para a pesquisa clínica. Tem exigido que uma equipe enorme se especialize na regulação ético-regulatório, síntese de produtos fabricados com condições de boas práticas de manufatura e arranjo com a indústria”, complementa o estudioso, ao citar Funed, Hipolabor e Ouro Fino como parceiras no desenvolvimento do imunizante contra Covid-19.
Trajetória de sucesso
Para chegar a esta penúltima fase da última etapa, a SpiN-TEC já passou por vários e criteriosos estágios, todos realizados em boas práticas laboratoriais.
Em outubro de 2022, a Anvisa liberou o teste clínico da vacina. Em novembro, recebeu o sinal verde do sistema CEP/Conep, formado pela instância máxima de avaliação ética em protocolos de pesquisa com seres humanos e os Comitês de Ética em Pesquisa.
Quando chega aos postos?
Após realizar as fases 1 e 2 dos testes clínicos, o grupo que desenvolve a SpiN-TEC vai mandar tudo o que foi observado em relatórios e solicitar autorização para a última fase da atual etapa: a terceira, cujo teste é feito em cerca de 5 mil voluntários.
Se tudo transcorrer sem imprevisto algum (a Anvisa pode, por exemplo, pedir que algum aspecto do teste seja refeito), é possível que a vacina 100% brasileira contra Covid-19 já comece a ser aplicada, de fato, em 2025.
“Demora, em média, de 20 a 30 anos para uma vacina ser desenvolvida. Lógico que a pandemia fez com que esse desenvolvimento fosse muito abreviado. Mas continua sendo um desenvolvimento muito rápido, já que os estudos da SpiN-TEC começaram em 2020”, afirma Helton Santiago.
“É um marco para a ciência brasileira e, reforço, com o desenvolvimento com um tempo muito bom. Não à toa é a primeira vacina 100% brasileira a chegar a esse estágio de desenvolvimento”, finaliza.